将来、私たちが何気なく口にしている朝のコーヒーが、がんや糖尿病に対する精密な遺伝子治療を「オン」にする引き金になるかもしれません。
カフェインを利用して、細胞内の遺伝子編集技術CRISPRを作動させる新しいシステムが発見されました。
この研究は、カフェインを外部スイッチとして利用し、設計された細胞内でのみ遺伝子編集を開始させることを可能にする点で大きな注目を集めています。
今回のテーマはそんなカフェインとがんについての研究です。
参考記事)
・Your morning coffee could one day help fight cancer(2026/03/02)
参考研究)
・Reprogramming chemically induced dimerization systems with genetically encoded nanobodies(2025/10/20)
カフェインで遺伝子編集を起動する仕組み

本研究を主導したのは、テキサス州に拠点を置くバイオサイエンス分野の研究機関でディレクターを務めるYubin Zhou氏です。
Yubin Zhouは、細胞レベル・遺伝子レベル・エピジェネティクスレベルで疾患を研究してきた研究者であり、これまでに180報以上の科学論文を発表しています。
彼は、CRISPRやケモジェネティクス(chemogenetics)といった最先端技術を用いて、複雑な疾患の理解と治療法の開発を目指してきました。
今回の研究の中心にあるのは、「ケモジェネティクス」という技術です。
これは、外部から投与される小分子(薬剤や食品成分など)によって、あらかじめ設計された細胞内スイッチを作動させる方法です。
従来の薬剤は体内のさまざまな組織に影響を及ぼす可能性がありますが、ケモジェネティクスでは特定の細胞だけが反応するように設計されている点が特徴です。
Zhouの研究チームは、CRISPR遺伝子編集技術とカフェインを組み合わせた新しいシステムを構築しました。
この仕組みでは、まず細胞に対して遺伝子導入を行い、3つの重要な構成要素を発現させます。
• カフェインに反応するナノボディ(抗体様分子)
• その標的となる対応タンパク質
• CRISPR編集機構
これらの遺伝子をあらかじめ細胞内に組み込んでおくことで、外部からの刺激に応答する準備が整います。
その後、ヒトが約20mg程度のカフェイン(コーヒー、チョコレート、炭酸飲料などに含まれる量)を摂取すると、ナノボディと標的タンパク質が結合します。
この結合が引き金となり、CRISPRが活性化され、特定の遺伝子編集が開始されるのです。
ここで用いられるカフェイン応答性ナノボディは「caffebody(カフェボディ)」と呼ばれています。
これは研究チームによる命名であり、一般的な学術用語として広く定着しているかどうかについては、現時点では明確ではありません。
T細胞を自在に制御する可能性
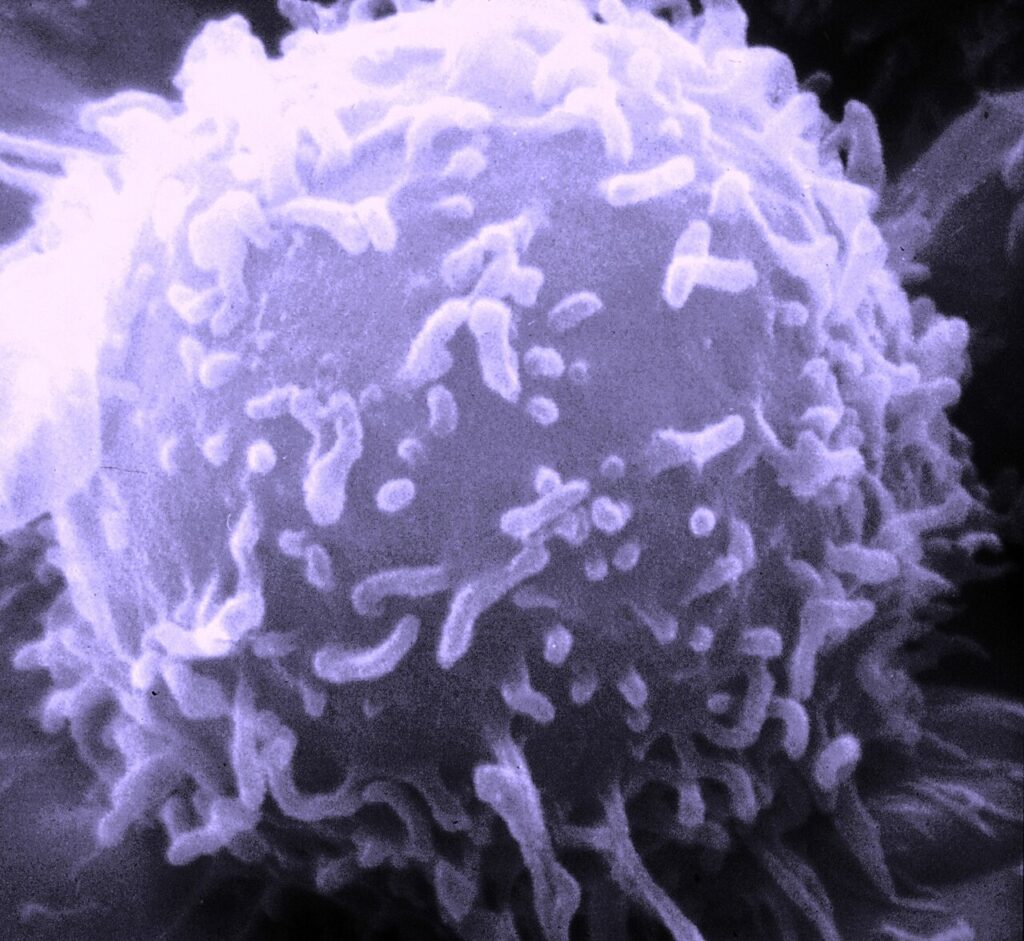
この技術の大きな応用先の一つが、免疫細胞であるT細胞です。
T細胞は、過去の感染情報を記憶し、再感染時に迅速に対応する役割を担う重要な細胞です。
今回のシステムでは、カフェインを用いてT細胞を意図的に活性化できる可能性が示されました。
これは、従来の遺伝子編集技術では難しかった制御方法です。
特にがん治療においては、キメラ抗原受容体T細胞療法(CAR-T療法)のように、患者自身のT細胞を改変して腫瘍を攻撃させる治療法があります。
この研究では、カフェボディを組み込んだCAR-T細胞にカフェインを投与することで、医師が攻撃のタイミングや強度を調整できる可能性が示唆されています。
ただし、これらの結果は主に実験室レベルおよび動物実験段階で得られたものであり、ヒト臨床試験で同様の効果が得られるかどうかは、今後の検証が必要です。
オンとオフを切り替えられる可逆的システム
本研究のもう一つの重要な発見は、遺伝子の編集を「止める」ことができる点です。
特定の薬剤を投与すると、結合していたタンパク質が解離し、CRISPR活性が停止します。
ここで注目されているのが、免疫抑制薬であるラパマイシン(Rapamycin)です。
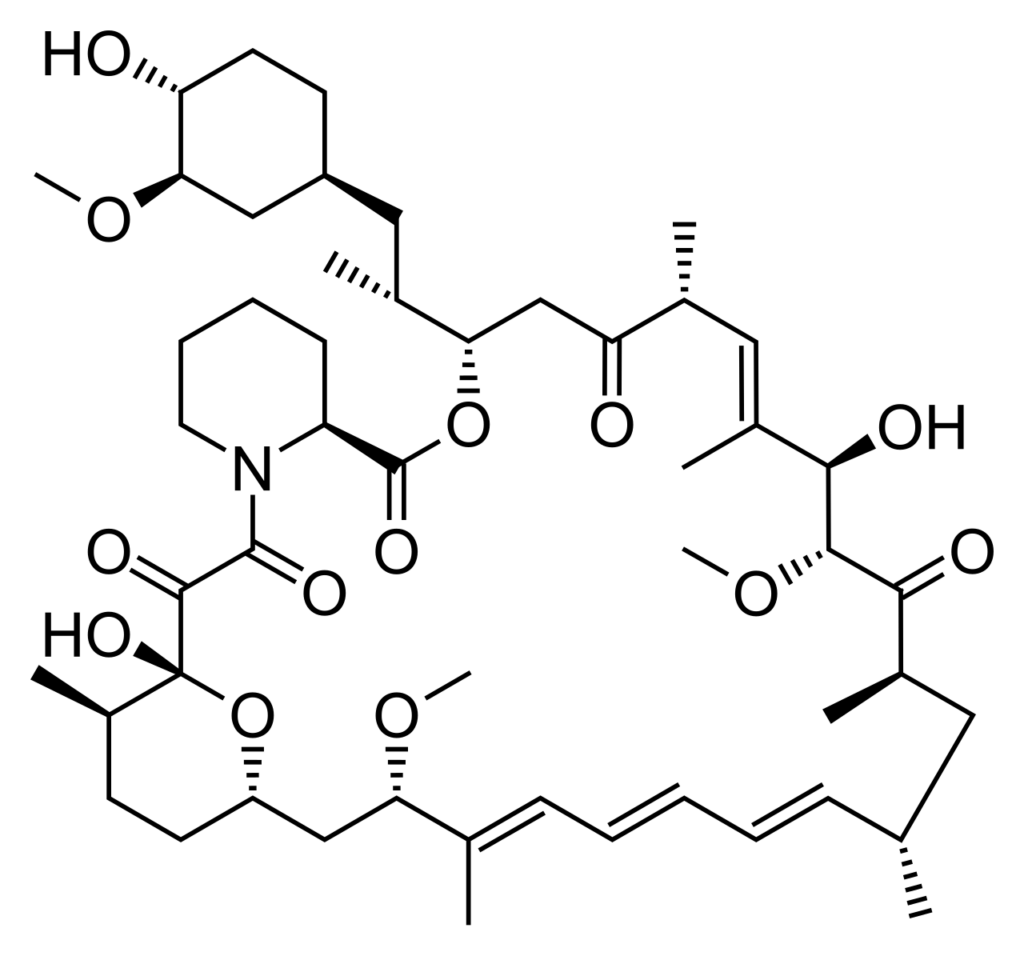
ラパマイシンは、臓器移植後の拒絶反応を防ぐために広く使用されてきた既存薬です。
この薬剤を利用することで、カフェインで開始した遺伝子編集を停止させることが可能になると報告されています。
Zhou氏によれば、タンパク質AとBが離れている状態でカフェインを加えると結合し、逆に結合している状態でラパマイシンを加えると解離させることができるとのことです。
このように、開始と停止の両方を外部から制御できる点は、現在の遺伝子制御技術の中でも極めて高い精密性を持つ可能性があると考えられます。
ただし、この制御が臨床環境で安全かつ安定的に機能するかどうかについては、まだ前臨床段階であり、実際の医療応用までには慎重な検証が必要です。
糖尿病治療への応用の可能性
研究チームは、このシステムをインスリン分泌制御にも応用できる可能性を示唆しています。
将来的には、糖尿病患者がコーヒーを飲むことでインスリン産生を増加させる細胞を活性化するという構想も描かれています。
さらに、このプラットフォームはインスリン以外の治療用分子にも応用可能です。
T細胞調節因子やその他の治療遺伝子の発現を、カフェインやラパマイシンの投与によって微調整できる可能性があります。
動物実験では、カフェインだけでなく、その代謝産物であるテオブロミン(チョコレートやココアに豊富に含まれる)もCRISPR活性化を引き起こすことが確認されたと報告されています。
ただし、これらの結果がヒトにそのまま適用できるかどうかについては、現時点では不確実性があります。
精密医療への新たな道
これまでにも小分子を用いて遺伝子編集を制御する試みは存在しましたが、本システムは数時間単位というカフェイン代謝時間に基づいた「時間窓」を利用して制御できる点が特徴です。
さらにラパマイシンを停止信号として用いることで、遺伝子編集の開始と終了を協調的に管理できるという利点があります。
Zhouは、このシステムをCRISPRやCAR-T細胞療法に統合できる「モジュール型プラットフォーム」と表現しています。
既存の食品成分や既承認薬を「制御信号」として再利用するという発想は、実用化へのハードルを下げる可能性があります。
ただし、本研究の多くは前臨床段階にあり、ヒトでの安全性、有効性、長期的影響については未検証の部分が残されています。
したがって、将来的な医療応用については慎重な評価が必要です。
まとめ
・カフェインを利用してCRISPR遺伝子編集を外部から制御できる新しいケモジェネティクスシステム(遺伝子工学と薬理学を組み合わせた技術)が開発された
・ラパマイシンを用いることで遺伝子編集を停止できる可逆的なオン・オフ制御が可能であると報告されている
・がん免疫療法や糖尿病治療への応用が期待されているが、現段階では主に前臨床研究であり、ヒトでの有効性は未確定


















コメント