塩素

塩素は反応性が高く、自然界では化合物として存在することがほとんどです。
代表的なものは塩として知られる塩化ナトリウムがあります。
胃酸の大切な成分としても働く大切なミネラルでもあります。
今回はそんな塩素について触れていこうと思います。
毒ガスとしての塩素

単体の塩素は毒性が強く、刺激臭のある有毒な気体です。
第一次世界大戦下ドイツ軍が塩素ガスを使用し、たった1日で5000人以上の死者を出すほどの毒性があります。
これに対抗し、塩素を中和する次亜塩素酸のマスクが開発されたりと対抗手段も編み出されていきました。

その後、報復としてフランス軍がホスゲン(炭素と酸素と塩素の化合物)ガスをドイツ軍に対して使用。
更にドイツ軍がより効果的な毒ガスや化学兵器を開発するなど、結果として毒ガス・化学兵器の有用性が明らかになりました。
第一次世界大戦終了までに30種類以上の化学兵器が開発されましたが、ジュネーヴ議定書によってガスや細菌学的な兵器の使用が禁止されました。
消毒としての塩素

毒性の強い塩素ですが、強い殺菌力と酸化作用を利用して消毒剤としても使われています。
水道水の原料となる河川や湖の水には様々な種類の微生物が存在します。
この水に一定量の塩素を混ぜることで、人間の害となる菌や微生物を殺菌しています。
各国の法律によって、水道水には微量の塩素を含めることが義務付けられ、これにより多くの国々で伝染病の蔓延が食い止められました。
その他身近なものでは塩素系の漂白剤などでも使われています。
漂白や除菌で高い効果を発揮しますが、酸性の物質と混ざることで塩素ガスが発生するので注意が必要になります。
塩素の製法
そんな塩素の代表的な製法がコチラ。
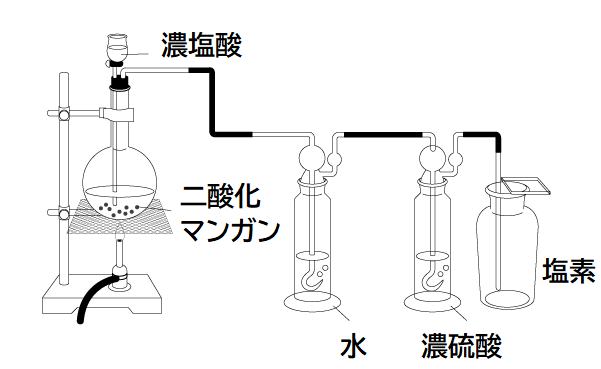
濃硫酸に二酸化マンガンを加えて熱すると、塩化マンガンと水と塩素に分かれます。
4HCl+MnO2
↓
MnCl2+2H2O+Cl2
しかし、気体として出てくるのは塩素だけでなく、あまった水素と塩素が化合した塩化水素や水蒸気が含まれます。
これらを取り除くために、水→濃硫酸の順に気体を通していきます。
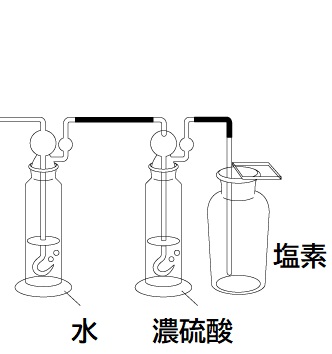
【水に通す】
塩化水素は水にとても溶けやすい性質があります。
ここで塩化水素が吸収されていきます。
(ちなみに塩化水素を吸収した水は塩酸になっていきます。)
【濃硫酸に通す】
前回の科学(科学)硫黄の記事にて、濃硫酸は水を吸収する性質(吸湿性)があることを説明しました。
濃硫酸(H2SO4)を通すことで気体と一緒に出てくる水蒸気(H2O)を吸収することで、最後は純粋な塩素を取り出すことができるのです。



















コメント