リンと身体
人体においてカルシウムに次いで多いミネラルがリン(Phosphorus)です。
体内ではほとんどのリンが酸素と結合しリン酸を形成しています。
また細胞膜、DNAを構成するヌクレオチドなど、いくつかの重要な物質の構成要素になっています。
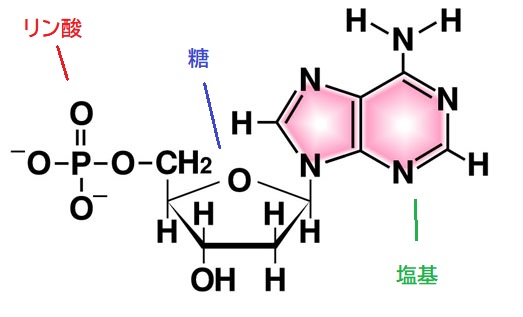
85%は骨に存在し、残りは細胞内でエネルギー生産に関わっています。
【高リン血症】
腎臓の機能が低下すると体内のリンの排出機能が働かず、高リン血症になることがあります。
多くの場合は症状は感じられませんが、血中のカルシウムと結合し、低カルシウム血症を引き起こしてしまうこともあります。
低カルシウム血症になると、痛みを伴う筋肉の痙攣や骨がもろくなるなどの障害が現れます。
【低リン血症】
また重度のアルコール依存症や重度の熱傷、飢餓による栄養の低下などの特別な条件化では、症状の回復の過程で多くのリンが消費されます。
体内のリンが必要以上に消費されると、低リン血症を引き起こします。
低リン血症が起こると、筋力低下、昏迷、昏睡と症状が悪化し死に至ります。
リンを多く含む食べ物としては、チョコレートや牛乳、卵黄などが挙げられます。

リンと植物

窒素、カリウム、リン酸とともに植物の3大肥料に数えられます。
植物の開花や結実の促進、発芽や根っこのつきをよくする働きがあり、 果実の成熟や品質の向上にも役立っています。
リン酸が欠乏すると、新しい葉っぱは小さくなり茎も細く、できた実の甘みが少なくなるなど品質の低下が見られます。

リンの同素体
白リンや赤リンなど同素体(同じ元素から成り、性質や構造の異なる単体が2種類以上存在するもの)を成し、他の元素と合わせてSCOPで覚えることができます。
S:斜方硫黄・単斜硫黄・ゴム状硫黄
C:ダイヤモンド・フラーレン・グラファイト(黒鉛)
O:酸素・オゾン
P:赤リン・黄リン

【白リンと赤リン】
白リン(別名黃リン)の発火点は約30~60℃と低温で、簡単に発火してしまうため水中で保存されています。
湿った大気中だと水分を吸収し、自動酸化反応で光を放ちます。
照明効果と燃焼効果から、煙幕弾や砲弾など(白燐弾)としても使われていました。

白燐弾の火薬が皮膚につくと、脂溶性の高さからすぐに皮膚内に浸透し重度の火傷を引き起こします。
この火傷による熱傷は治療が難しく非人道的であるため、これに類する兵器は現在では使用が禁止されています。
発火点が約260℃と空気中に置いても自然発火しない赤リンは、マッチや花火の原料として使われています。
かつてはマッチの頭薬に白リンが使われていたこともありましたが、案の定事故が多発。
現在では毒性もなく安全な赤リンに置き換わっています。




















コメント