私たちの体内、とりわけ腸で何か問題が発生すると、その影響を即座に感じることがあります。
2024年11月にASM(アメリカ微生物学会)ジャーナルにて掲載された研究から、有害な細菌がどのようにして腸内で痛みを引き起こし、腸の内容物を排出させる防御反応を誘発するのかが明らかになりました。
オレゴン大学とカリフォルニア大学アーバイン校の研究者たちは、特にコレラ菌(Vibrio cholerae)に注目し、この防御反応の仕組みの解明を試みました。
この細菌は下痢性疾患の原因菌として広く知られており、以前の研究ではコレラ菌がゼブラフィッシュの腸内で収縮を引き起こすことを確認していました。
今回はそのメカニズムをさらに詳細な調査から、腸内の物理的な変化が主要な役割を果たしていることが分かりました。
以下に研究の内容をまとめていきます。
参考記事)
・Harmful Bacteria Can Trigger Pain in Your Gut, And Now We Know How
(2025/01/12)
参考研究)
・The Vibrio type VI secretion system induces intestinal macrophage redistribution and enhanced intestinal motility(2024/11/22)
腸内細菌が引き起こす炎症と腸の働きへの影響
ゼブラフィッシュをモデルにした研究では、腸内細菌が免疫細胞や腸の機能に及ぼす影響について解明されました。
特に注目されたのが、免疫系の炎症性サイトカインである「TNFα(腫瘍壊死因子α)」とその役割です。
このサイトカインは、細菌感染時に腸内で重要な防御反応を引き起こす一方、腸の過剰な収縮や炎症による不快な症状にも関与していることが明らかになりました
TNFαの役割と腸炎症の仕組み
研究では、腸内に存在するビブリオ菌(Vibrio ZWU0020)が、免疫細胞の一種であるマクロファージを活性化させ、TNFαの分泌を促すことが確認されました。
このTNFαが腸内で以下のような一連の反応を引き起こします。
1. 腸壁の炎症
TNFαの放出により腸壁が炎症を起こし、組織が損傷する
損傷部位には免疫細胞であるマクロファージが集まり、修復を試みますが、これが炎症をさらに悪化させる場合もある
2. 腸神経の異常活性化
炎症やTNFαの影響で腸内神経が刺激を受け、過剰に反応する
この結果、腸が強く収縮し、内容物を速やかに排出する反応が起こる
3. 腸の防御メカニズム
腸が異物や有害な細菌を迅速に体外へ排出する仕組みは、体を守る重要な防御反応として機能する、炎症による痛みや腸収縮による不快感が伴う
これらのメカニズムが明らかになったことで、腸内細菌が免疫と神経を介して腸機能に大きな影響を及ぼしていることが示されました。
この発見は、炎症性腸疾患(IBD)などの治療法開発への応用が期待されています。
ゼブラフィッシュを用いた観察

ゼブラフィッシュの幼生は体が半透明であるため、体内の細胞や神経、腸の動きをリアルタイムで観察できる利点があります。
また、ゼブラフィッシュの免疫系は人間と非常に似ており、この研究で得られた知見が人間の腸にも応用可能であることを示唆しています。
観察では、腸壁が損傷を受けるとマクロファージが損傷箇所に急行する様子が確認されました。
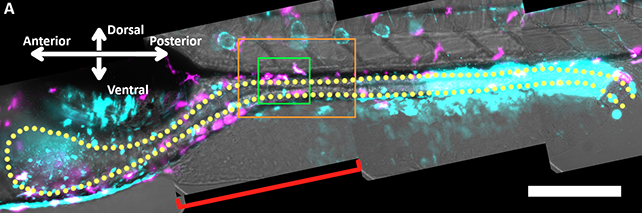
この際、マクロファージが通常果たす腸神経の制御機能が一時的に失われるため、腸神経が過剰に反応して腸収縮が引き起こされます。
この反応によって腸内の内容物が排出される仕組みは、防御メカニズムとして働く一方、過剰な収縮や炎症を伴うことで不快な症状を引き起こします。
研究者たちはゼブラフィッシュ内でのダイナミックな細胞活動に驚きを示し、腸の収縮や免疫細胞の動きを追跡する技術の重要性を強調しています。
また、「この技術がなければ、今回の腸内環境の仕組みを解明することはできなかった」と述べています。
体を守る防御反応と細菌の策略
腸の痛みや収縮は一見すると不快な症状ですが、腸内に侵入した細菌や有害物質を迅速に排出するための重要な防御反応です。
この反応は腸内環境を整える役割を果たす一方、コレラ菌などの病原菌がその仕組みを利用して他の細菌を排除し、自身の拡散を助ける場合もあります。
研究者たちは、コレラ菌特有の活動ではなく、腸の損傷時に起こる普遍的な反応であることを指摘しています。
腸は損傷を受けると、それを洗い流す仕組みがデフォルトとして機能するのです。
このような防御反応を理解することは、炎症性腸疾患の治療法開発にも大きな意義を持ちます。
今後の研究の方向性
今回の研究では、腸内細菌、免疫系、神経系がどのように連携して体を守るかについて新たな知見が得られました。
しかし、腸内環境を完全に解明するにはさらなる研究が必要です。
特に、免疫系と神経系の相互作用を詳細に調べることで、新しい治療法の開発が期待されています。
また、今回の発見はコレラ菌以外の細菌にも適用可能であり、広範囲の腸疾患の理解と治療に貢献する可能性があります。
今回の成果は、腸内の免疫と神経の複雑な関係を深く理解する一歩となり、私たちの健康維持にとって重要な洞察をもたらしました。
まとめ
・コレラ菌が腸に物理的損傷を与え、マクロファージが損傷箇所へ移動することで腸内神経の活性化を引き起こす
・TNFαは腸内細菌が引き起こす炎症反応の中心的な役割を果たし、腸の収縮や防御反応を促進する
・腸の収縮と痛みは、体内の潜在的な脅威を排出する防御反応として機能する
・今回の発見は他の細菌にも適用できる可能性があり、炎症性腸疾患などの治療法開発に役立つことが期待されている
コメント