地上に当たり前存在し、私たちの生活に欠かせない水。
以前の記事↓に続き、今回も水の不思議について学んでいきます。
水素同士の結合
水の不思議な性質は、水分子の形が原因です。
ご存じの通り、二つの水素原子と一つの酸素原子で構成される水分子。

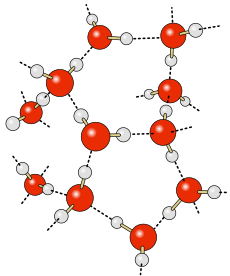
水分子の内部では、電子が均等に分布していないので、水素原子(白い部分)には+の電荷、酸素原子(赤い部分)には-の電荷を帯びる。
+と-は引きつけ合うため赤の部分は白に、白の部分は赤にくっつく。
これが水素結合というワケです。
氷と水の違い
氷では水分子が安定的に結合して正四面体を作ります。
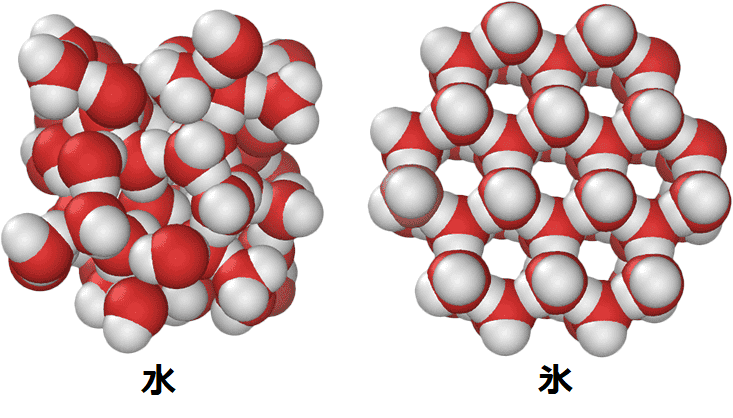
氷になる過程で四面体がくっつき合って、規則的な塊になると微妙に隙間ができ密度が小さくなります。(下図の右)
水(下図の左)よりも密度が小さくなるため、氷は水に浮いてしまうのです。
個体の氷は安定的に結合していますが、液体の水は水素結合が形成されたり壊れたりを繰り返します。
水素結合の平均寿命はなんと一兆分の一秒程度にしかないのです。
表面張力の発生
水分子同士がお互いに引っ張り合い集まろうとする性質があるため、はなるべく表面積を小さくしようとします。
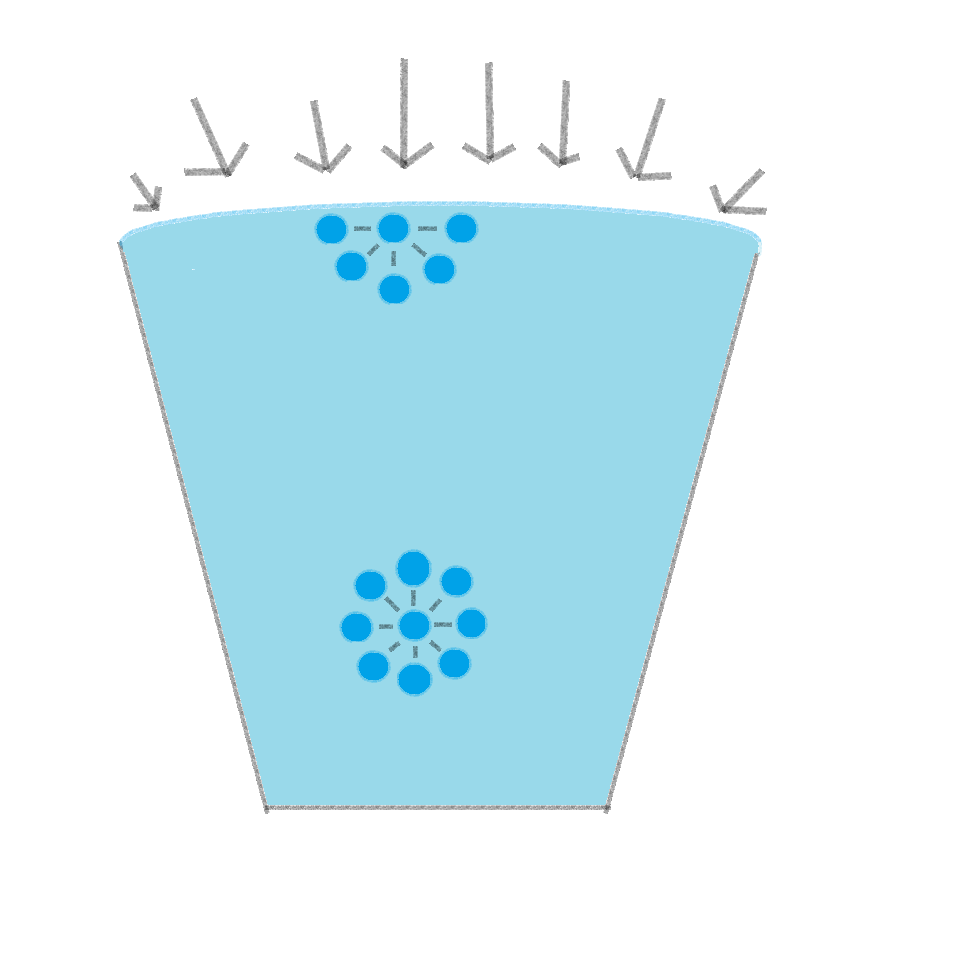
コップの真ん中の水は四方八方から均等に引っ張り合いますが、コップの表面でも同じ動きをしようとします。
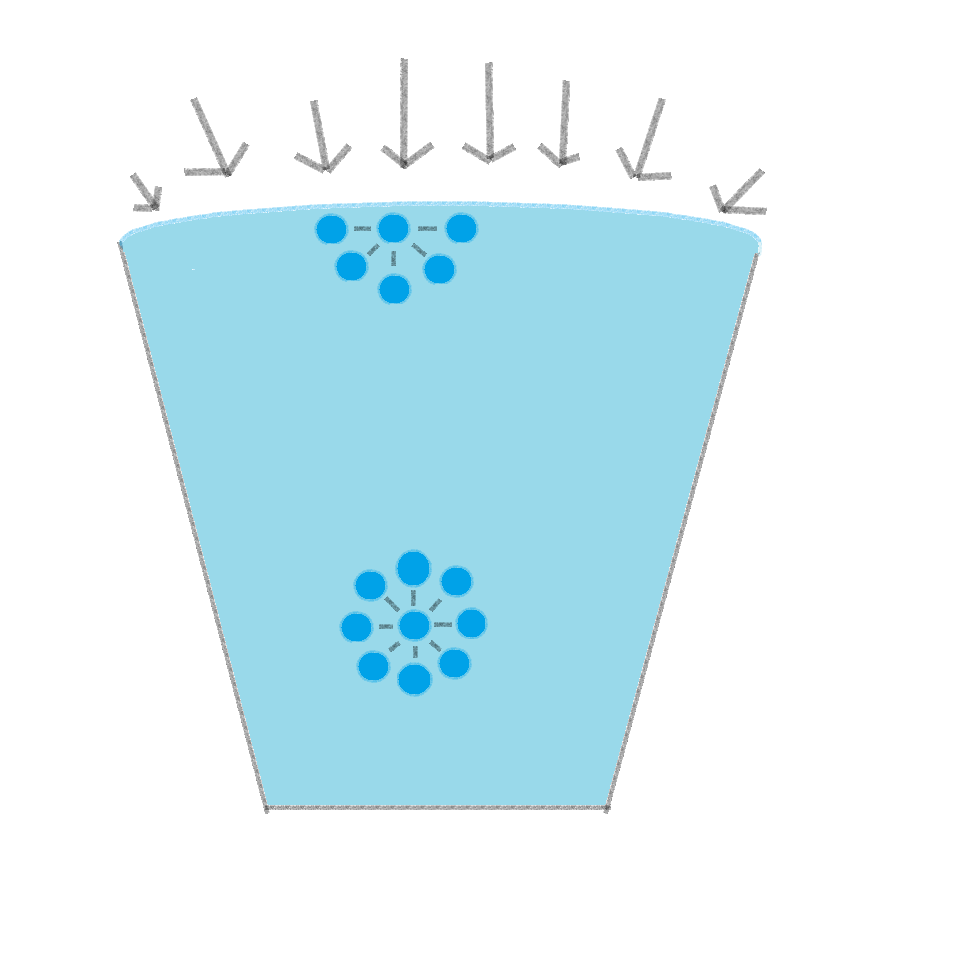
この集まる性質と表面積をできるだけ小さくしようとする働きが、表面張力を発生させるのです。
水の表面張力は比較的強く、水面に落ちた虫の羽程度でしたら身動きが取れないくらい引っ張る力があるのです。


コメント